Asitlik ve Bazlık Özellikleri
- Bir periyotta soldan sağa doğru ve bir grupta aşağı- dan yukarıya doğru element oksitlerinin asidik ka-rakteri artar.
- Bir periyotta sağdan sola doğru ve bir grupta yuka- rıdan aşağıya doğru element oksitlerinin bazik ka- rakteri artar.
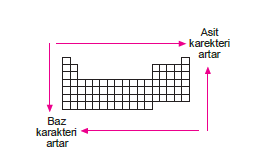
- Periyodik özellikleri grup ve periyotlara göre aşağı- daki biçimde özetleyebiliriz
Gruplarda yukarıdan aşağı inildikçe
- Atom numarası artar.
- Atom çapı artar.
- İyonlaşma enerjisi azalır.
- Elektronegatiflik azalır.
- Elektron ilgisi azalır.
- Element oksitlerinin bazik karakteri artar.
- Değerlik elektronları sayısı değişmez (8A grubu ha- riç).
Periyotlarda soldan sağa gidildikçe
- Atom numarası artar
- Atom çapı azalır.
- İyonlaşma enerjisi artar.
- Elektronegatiflik ve elektron ilgisi artar.
- Element oksitlerinin asidik karakteri artar.
- Değerlik elektronları sayısı artar.
BİLEŞİK oluŞUMU
Elementler birbirleriyle birleşerek bileşikleri oluştururlar. Atomlar elektron alarak, vererek veya ortak kullanarak kararlı yapıya (soygaz elektron yapısı) ulaşmak isterler.
Metal atomları ametal atomları ile iyonik bileşik, ametal atomları ise kendi aralarında kovalent bileşik yaparlar.
- Elementlerin gruplarına göre, bileşiklerinde alabileceği değerlikler aşağıda verilmiştir.
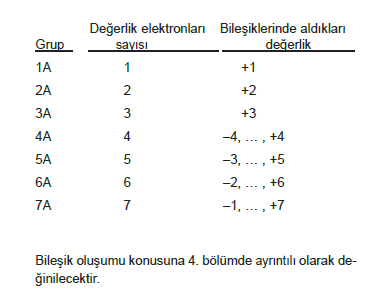
Bileşik oluşumu konusuna 4. bölümde ayrıntılı olarak değinilecektir.
NOT: En kuvvetli iyonik bağlı bileşik, en aktif metal (7.periyot 1A grubu) ile en aktif ametal (2. periyot 7A grubu) arasında oluşur.
