Elektrokimyasal Piller

Kimyasal enerjiyi, elektrik enerjisine dönüştüren düzeneklere elektrokimyasal pil denir. Elektrokimyasal pillerde yükseltgenme ve indirgenme yarı tepkimeleri iki ayrı kapta oluşur. iki kap arasındaki elektron akışı bir iletken telle sağlanır.
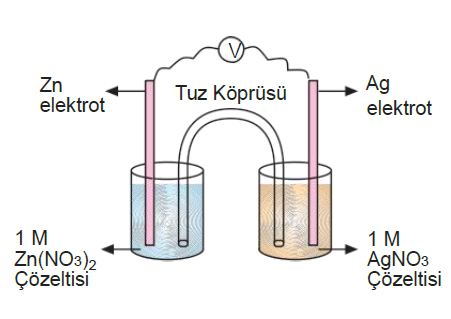
Çözeltilerin içine konulan metal çubuklara elektrot denir. Elektrotlar, voltmetre üzerinde iletken tel ile birbirine bağlanır. İyon hareketini sağlamak amacıyla iki kap ara- sına tuz köprüsü koyulur. Tuz köprüsü, içinde KNO , KCl3 gibi çözeltiler bulunan ters U borusudur.
Zn nin yükseltgenme eğilimi Ag den fazla olduğu için Zn 2e vererek yükseltgenir. Zn elektrotun kütlesi zamanla azalır. Çözeltide Zn+2 iyonu derisimi artar.
Zn (k) Æ Zn+2 (aq) + 2e– (yükseltgenme yarı tepkimesi)
Ag+ iyonları eletron alarak indirgenir. Çözeltide Ag+ iyonu derisimi azalır. Ag elektrot üzerinde metalik Ag birikir. Ag elektrodun kütlesi artar.
Ag+ (aq) + e– Æ Ag (indirgenme yarı tepkimesi)
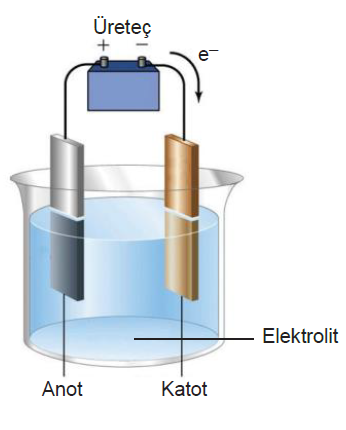
Elektrokimyasal pillerde yükseltgenmenin gerçekleştiği elektroda anot, indirgenmenin gerçekleştiği elektroda katot denir.
Buna göre Zn elektrot anot, Ag elektot katottur. Toplam pil tepkimesi yazılırken indirgenme yarı tepkimesi ile yükseltgenme yarı tepkimesi taraf tarafa toplanır.
Tepkimelerde alınan ve verilen elektronlar eşit olmalıdır.
Bu yüzden indirgenme yarı tepkimesi 2 ile çarpılır.
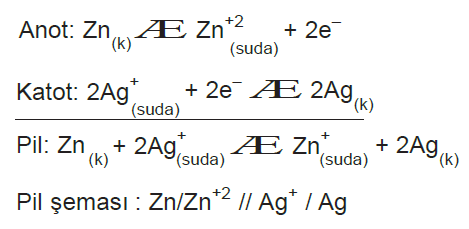
şeklinde ifade edilebilir.
Pil çalışırken anot bölmesinde Zn+2 derişimi arttığı için (+) yük fazlalığı oluşur. Katot bölmesinde Ag+ derişimi azaldığı için (–) yük fazlalığı oluşur. Yük denkliğini sağlamak amacıyla tuz köprüsünden anyonlar anod, katyonlar katoda doğru hareket eder.
- Pil çalışırken tuz köprüsünden anyonlar anoda, katyonlar katoda göç eder.
- Pilde elektron akışı anottan katoda doğrudur.
Standart Pil Gerilimi
Sıcaklığın 25°C, basıncın 1 atam ve iyon derişimlerinin
1M olduğu şartlarda (standart şartlar) ölçülen pil gerili- mine standart pil gerilimi(potansiyeli) denir. Hidrojen elektrodun standart koşullarda gerilimi 0,00 volt kabul edilip hangi yarı pilin gerilimi saptamak isteniyorsa, standart hidrojen yarı piline bağlanarak pil oluşturulur.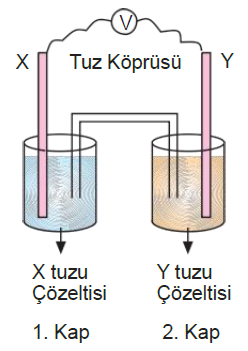
Standart pil gerilimleri E° ile gösterilir.
Bir yarı tepkime ters çevrilirse E° değerinin işareti deği- şir. Yarı tepkime denklemi herhangi bir sayı ile çarpılırsa E° değeri değişmez.
Pil gerilimi indirgeme potansiyeli ile yükseltgenme potan- siyelinin toplanması ile bulunur.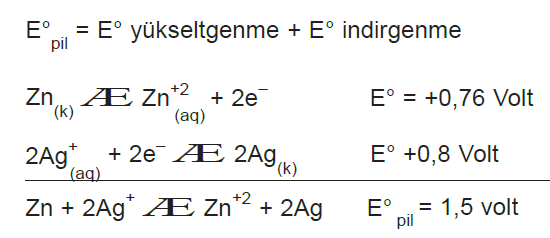
Yükseltgenme potansiyeli büyük olan elektrot anot, küçük olan elektrot katottur.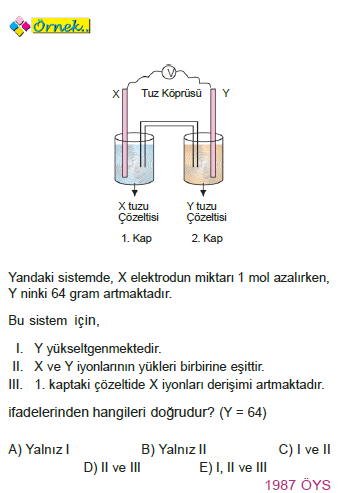
ÇÖZÜM: X elektrodun miktarı azaldığına göre,X elektrot yükseltgeniyordur. Y indirgenir Y nin miktarı 64 g artmaktadır. X 1 mol azalırken Y 1 mol artıyorsa X ve Y nin yükleri eşittir. X anot olduğu için 1. kapta X iyonları derişimi artar.
Yanıt D

