enerji seviyeleri
- Atomların belli frekanslarda elektromagnetik ışıma yapması,atomun sahip olacağı enerji değerlerinin kesikli olduğunu gösterir. Atomun sahip olabileceği bu iç enerjilere enerji seviyeleri denir.
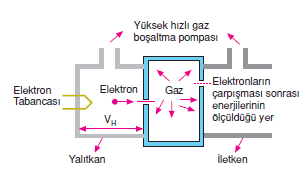
- Elektron tabancasından fırlatılan elektronlar VH gerilimi ile hızlandırılarak gaz atomlarının bulunduğu odaya gönderilir.
- Gaz atomlarıyla çapışma yaptıktan sonra çarpışma sonrası enerjilerinin ölçüldüğü diğer odaya geçerler.
- Elektronların gaz odasına girdiği ve çıktığı aralıklar karşılıklı değildir. Bunun nedeni elektronların gaz atomlarınaçarparak çıkmasını sağlamaktır. Yüksek hızlı gaz boşaltma pompaları diğer odaya kaçan gaz atomlarını boşaltmaktır.
- VH gerilimi ile Ek enerjisi kazandırılan elektronların son odada da enerjileri ölçülür.
- Elektronların gaz odasına girişteki ve çıkıştaki enerjileri farkı kaybettiği enerjiyi verir. Bu çarpışma sonucu atoma verilen enerjidir.
- Gaz odasında civa buharı varken enerjisi 4.86 eV olan elektronlar gönderildiğinde, çıkan elektronların 4.86 eV enerji kaybettiği görülür.
- Bir atom tarafından alınabilecek en küçük enerji miktarına o atomun birinci uyarılma enerjisi denir. Civanın 1.uyarılma enerjisi 4.86 eV dır.
- Civa atomunun alabileceği enerji miktarını çıkan elektronların son kinetik enerjilerini ölçerek bulabiliriz. Civa atomunun bazı enerji düzeyleri aşağıdaki gibidir.

- Uyarılma enerjisi verilmeden önce atomun içinde bulunduğu hale temel hal denir. Temel halin üzerinde birinci uyarılma enerjisi ve diğer uyarılma enerjileri yer alır. Atoma
- 10.4 eV enerji verdildiği zaman atomdan bir elektron kopar ve geriye pozitif yüklü bir iyon kalır. Atomu iyonlaştıran bu enerjilye iyonlaşma enerjisi denir.
- Enerji seviyeleri her atom için farklıdır. Üstt enerji seviyesine çıkan atom yaklaşık on üzeri sekiz s de aldığı enerjiyi ışık fotonu olarak yayınlayarak alt enerji seviyelerine ya da temel hale geçer.
- Yayınlanan fotonların enerjileri bu iki seviye arasındaki enerji farkı kadar olur.
bohr atom modeli
- Bu atom modeli 1910 yılında Niels Bohr tarafından geliştirilmiştir.
- Ortaya attığı üç postülatla elektronların çekirdek çevresinde belli dairesel yörüngelerde dolandığını,enerji kaybederek çekirdeğe düşmediğini ve ivmeli hareketten dolayı enerjilerinin kesikli oluşunu açıklamıştır.
Bohr Postülatları
1. Çekirdek çevresinde elektronların yörüngelerinin çapı belli değerlerdedir. m kütleli elektronun V hızıyla hareket ederken elektrona eşlik eden de Brogli dalga boyu![]()
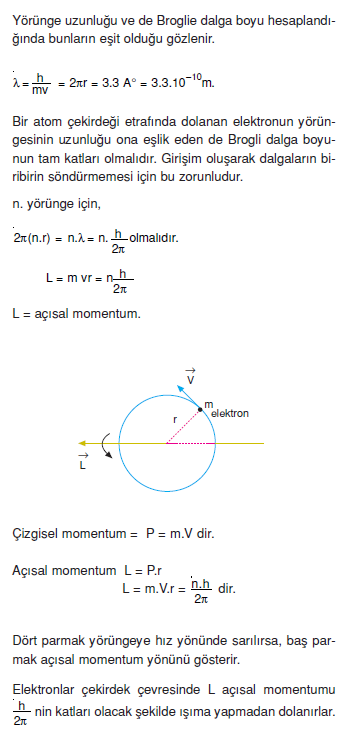
2. Elektronlar çekirdek çevresinde dönerken kararlıdırlar.
- Belli yörüngelerde belli enerjilere sahiptirler.
- Enerji kaybederek çekirdeğe düşmezler.
3. Elektron yörüngeler arasında geçiş yapabilir.
- Yüksek enerjili kararlı bir yörüngeden, düşük enerili kararlı herhangi bir yörüngeye kendiliğinden geçebilir.
- Bu geçişte ortaya çıkan enerji Eilk – Eson yayınlanan fotonunun enerjisi olur.

Bohr yörünge yarıçapı
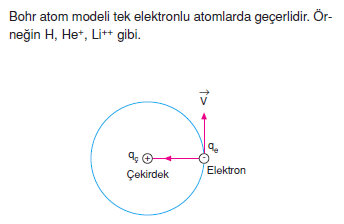
- Elektron kararlı yörüngede dolanırken merkezcil kuvvet ve coulomb çekim kuvveti etkisinde kalır. Elektron düzgün dairesel hareket yaptığına göre coulomb kuvveti merkezcil kuvvete eşittir.
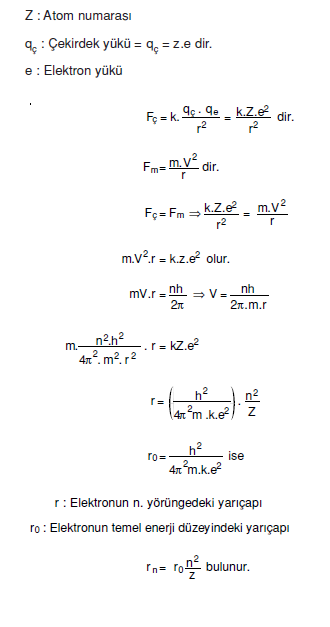
Bohr Yörünge Hızı ve Enerjisi
Bohr yörüngesinde dolanan elektronun hızı




