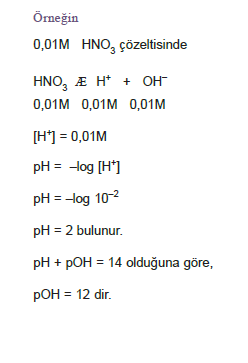
Kuvvetli Asit ve Bazlarda pH ve pOH
Kuvvetli asit ve bazlar suda tamamen iyonlaştıklarından çözelti derişiminden H+ ve OH– iyonlarının derişimi bulu-nabilir.
ÖRNEK :0,4 gram NaOH katısı 10 L suda çözülüyor.
Oluşan çözeltinin pH değeri kaçtır? (NaOH = 40)
A) 3 B) 5 C) 10 D) 11 E) 13
ÇÖZÜM: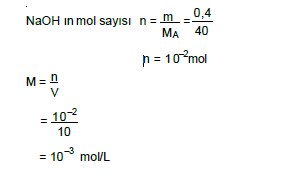

Zayıf Asit ve Bazlarda pH ve pOH
Zayıf asitler tamamen iyonlaşmadığı için iyonlaşmamış asit ve iyonlar arasında bir denge söz konusudur.


ÖRNEK:Oda sıcaklığında HNO2 nin asitlik sabiti (Ka) 4×10 , HCN nin asitlik sabiti (Ka) 6×10–10 olarak verilmiştir.
Bu asitlerin aynı sıcaklıkta eşit derişimli sulu çözelti- leri ile ilgili,
I. HCN daha zayıf bir asittir.
II. HNO2 nin pH si daha büyüktür.
III. HCN nin iyonlaşma yüzdesi daha küçüktür.
yargılarından hangileri doğrudur?
A) Yalnız I B) Yalnız II C) Yalnız III D) I ve II E) I ve III
1996 ÖYS
ÇÖZÜM:Aynı sıcaklıkta Ka değeri küçük olan asit daha zayıftır. HCN daha zayıf olduğu için iyonlaşma yüzdesi daha kü- çüktür. İyonlaşma yüzdesi küçük olduğu için H+ derişimi küçük ise pH ı büyüktür. pH ı büyük olan HCN dir.
Yanıt E
[ad1]
Nötrleşme
Asit ve baz çözeltileri karıştırıldığında asitten gelen H+ iyonu ile bazdan gelen OH– iyonu tepkime verir. Bu tepkimeye nötrleşme denir.

Kuvvetli Asit – Kuvvetli Baz Titrasyonu
Derişimi bilinen bir baz çözeltisi ile derişimi bilinmeyen asit çözeltisinin derişiminin belirlenmesi veya derişimi bilinen asit çözeltisi ile derişimi bilinmeyen baz çözeltisinin derişiminin belirlenmesi işlemine titrasyon denir.
Örneğin derişimi bilinmeyen asit çözeltisinin, derişimi bilinen baz çölzeltisi ile titrasyonunu inceleyelim.
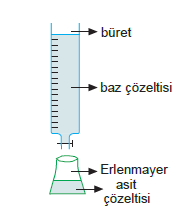
Şekilde görüldüğü gibi erlenmayere hacmi belli asit çö- zeltisi, bürete derişimi belli baz çözeltisi konur.
Nötrleşme anını tespit etmek amacıyla asit çözeltisine indikatör (ayıraç) eklenir.
Baz çözeltisinden damla damla asit çözeltisi üzerine eklenir. Nötrleşme anında indikatör renk değiştirir ve baz ilavesi durdurulur.
Bu ana dönüm(ekvalens) noktası denir. Dönüm noktasında, nH+ = nOH– (pH = 7) dir.
Bu olayla ilgili ilave edilen baz hacmine karşı pH derişimi grafiği
[m2]
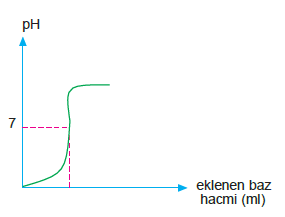
şeklinde olur.
Titrasyon eğrisinde pH ın 7 olduğu noktada,
Masit Vasit tasit = Mbaz Vbaz tbaz eşitliği yazılabilir.
M: Molar derişim (M) V: Hacim (L)
t: Tesir değerliği

[kimya_ygs_lys]

Kaçıncı sınıf bu?