Tepkime Hızına Etki Eden Faktörler
1. Maddenin cinsi
2. derişim ~ Basınç
3. Sıcaklık
4. Temas yüzeyi
5. Katalizör
1. Maddenin cinsi
1. Maddenin cinsi
Tepkime sırasında reaktif maddelerde bağ koparılıp yeni bağ oluşuyorsa tepkimeler yavaş, bağ kopması yoksa (iyonik tepkimeler) tepkime hızlıdır.

UYARI: Kopan ve oluşan bağları taşıyan molekül sayısı arttıkça tepkime yavaşlar
2. Derişim – Basınç
Tepkime kabının hacmi büyütülüp veya küçültülürse, birim zamandaki çarpma sayısı değişeceğinden tepkime hızı değişir.
hacim V≠ derişim MØ tepkime hızı azalır. hacim VØ derişim M≠ tepkime hızı artar.
Aynı hacimdeki kaba tepkimeye giren maddelerden her- hangi biri ve ikisi ilave edildiğinde, derişim artar. Dolayısıyla tepkime hızı artar.
NOT: Basınç artışı da gaz fazındaki madelere, derişimle aynı etkiyi yapar.
3. Sıcaklık
Sıcaklık arttırılırsa,
1. Kinetik enerji artar.
2. Eşik enerjisine sahip tanecik sayısı artar.
3. Tanecik hızı artar.
4. Etkin çarpışma yapan tanecik sayısı artar.
5. Birim zamanda çarpışan tanecik sayısı artar.
6. Aktifleşmiş kompleks sayısı artar.
7. Tepkime hızı artar.
8. Aktifleşme enerjisi değişmez.
NOT: Tepkime ister ekzotermik, ister endotermik olsun sıcaklık artışında tüm tepkimelerin hızı kesinlikle artar.
Sıcaklık etkisinin enerji dağılım eğrisi üzerinde incelenmesi: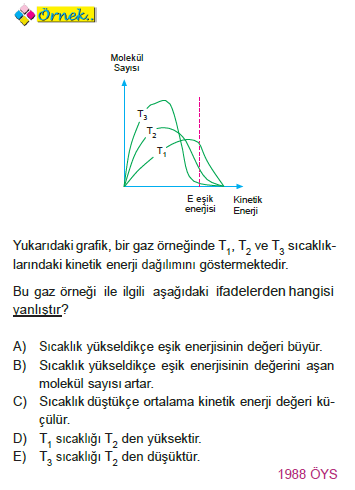
ÇÖZÜM: Grafikte eşik enerjisi sabit kalıp, eşik enerjisini aşan tanecik sayıları farklıdır. Eşik enerjisi düzeyi sıcaklığa bağlı değildir. Bu nedenle sıcaklığın artması ya da azalması eşik enerjisini değiştirmez. Eşik enerjisini katalizör değiştirir.
Yanıt A
4. Temas Yüzeyi

Heterojen tepkimelerde katı madde küçüldüğünde temas yüzeyi artar, bunun sonucu birim zamandaki çarpışma sayısı artacağından tepkime hızı artar.
Odun talaşının odundan daha hızlı yanması, plaka de- mirin, toz demirden daha geç paslanması bu yüzdendir.
ÇÖZÜM: Zn katısının miktarını ve temas yüzeyini artırmak H2 ga- zının miktarını ve hızını arttırır.
HCl çözeltisinin ise derişimi artırılırsa H2 gazının miktarı ve hız artar.
Yanıt A
5. Katalizör
Tepkime hızının artmasına neden olan maddedir. Yapı- lan işleme ise kataliz denir.
Özellikleri,
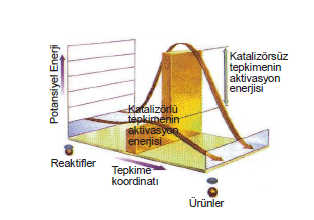
- Katalizör ΔH ı etkilemez.
- Aktifleşme enerjisini düşürür.
- Tepkime hızını artırır.
- Hız sabiti k nın sayısal değerini büyütür.
- Tepkimeyi hızlandırırken, ürün miktarını değiştir- mez.
- Tepkimeye katılır ve tepkime sonunda eksilmeden ortamda kalır.



müthiş bir onu sözlüden kesin 100 alacam
Bilgiler için teşekkürler.Çıkmış soruları vermeniz harika.Biraz karşılaştırma ve detay olsa daha iyi olur. Fazla bilgi göz çıkarmaz.
arkadaşlar AE diye aralarda gösterdiği nedir
aktifleşme enerjisi kardeşim
sıcaklık tepkime sabiti olan k’yı etkiliyor mu